Zeitgeist: Moving Forward (2011)
, PR-ammattilaiset, myyntiedustajat ja jopa lääkärit ovat usein epämääräisiä, kun uudet tuotteet osuvat markkinoille ja ovat saatavilla meille diabeetikoille. He keräävät uusia työkaluja "pian" ilman mitään erityisominaisuuksia siitä, milloin tuote saattaa todellisuudessa olla käytettävissä. Ja potilaiden suosimissa sanomalehdissä huhut voivat lentää.

Vuoden 2012 uuden diabetes-tuotteen hyväksyntävuoden jälkeen halusimme selvittää paremmin tämän kehityksen tilan ja myyjät ovat valmiita saamaan nämä uudet D-tuotteet käsiinsä .
Me kaikki tiedämme, että toisinaan katsomalla diabeteksen laitteiden esittelyjä ulkomailla on sellaista kuin peeringin kristallipalloa varten, mistä on tullut Stateside, mutta on silti vaikeaa kynsilata tiettyä aikajanaa ulkonäköä varten U. S.
Fellow D-Blogger Michael Aviad yli ASweetLife äskettäin koonnut listan seitsemästä uudesta D-tuotteesta, jotka odotetaan jossakin vaiheessa tänä vuonna. Kun kellonaika on nyt alkanut, ajatus oli syytä tarkastella täsmälleen kun jotkut näistä ja muista uusista tuotteista realistisesti odotetaan osuvan markkinoille.
Joten tässä on meidän todenmukaisuustarkistus, mitä odotamme vuonna 2013 (tai ainakin "sana" myyjiltä itseltään):
Muista nykyisin kuollut FreeStyle Navigator CGM (jatkuva glukoosinseurantajärjestelmä), joka Abbott palautti Yhdysvalloissa takaisin elokuussa 2011 (kun meidät johdettiin looong aika, että se oli vain "keskeytetty" vähän)? No, saimme sanaa lokakuussa EASD: n (European Association for Diabetes Study) konferenssin jälkeen, kun Abbott selvitti seuraavan sukupolven Navigatorin hiljaista käynnistämistä Yhdysvalloissa. Tänä aikana yhtiön julkisten asioiden johtaja ei kertonut virallista esittelyä tehtiin EASD: ssä, eikä mitään tapahtunut Yhdysvaltain käynnistämisen osalta.Mutta pysyimme utelias. Varsinkin kun olet oppinut FDA: n hyväksymästä kliinisestä tutkimuksesta täällä Santa Feissa, NM: ssä ja Atlanta, GA: ssä, mukaan lukien Navigator II. Ja sen jälkeen kun kuvat ja yksityiskohdat näkyvät verkossa yhtiön saksalaisella verkkosivustolla.
Tiesimme tämän uuden vuoden alusta PR-ohjaajalle Jeff Christensenille, ja hän kertoi meille:

"Kuten tiedätte, alkuperäinen FreeStyle Navigator System on lopetettu Yhdysvalloissa. Tämä tilanne jatkuu ennallaan. FreeStyle Navigator II -ohjelmaan, emme yleensä paljasta tietynlaista liiketoimintastrategiaa tai suunnitelmia, jotka koskevat sääntömääräisiä tiedostoja. Voin kuitenkin vahvistaa, että kehitämme edelleen seuraavan sukupolven tuotteitamme, jotka perustuvat Sensing-tekniikkaan, joka on FreeStyle Navigatorin ydin. < "Erityinen tutkimus, johon olet viitannut, liittyi 31 enrollees ja on valmis, kuten on merkitty Kliiniset tutkimukset.gov. Tietoja, joita meillä on käytettävissä tutkimuksessa, on se, mitä on lähetetty (siellä). "
Toki me saamme sen - tavaroita, joita et vain voi sanoa, mutta yritykselle, joka veti maton niin monilta lojaaleilta Asiakkaat, jotka ovat menettäneet alkuperäisen Navigatorin saatavuuden, toivoisimme hieman enemmän. Henkilökohtaisesti on vaikea nähdä, miten kukaan voisi katsoa Abbottin aiempien käyttäytymistapoja ja kirjautua yrityksen kanssa tulevaisuudessa … mutta kuka tietää. kaikki on riippuvainen laitteesta, ilmeisesti.
Christensen sanoo nyt, että Nav II on saatavana Belgiassa, Tanskassa, Ranskassa, Saksassa, Israelissa, Alankomaissa, Norjassa, Ruotsissa
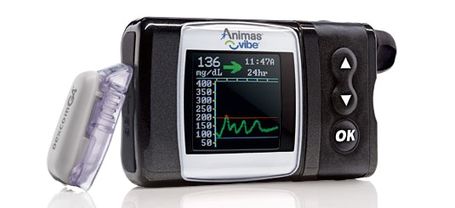
Animas Vibe Integrated Pump & CGM SystemJokainen on odottanut seuraavaan integroituun pumppuun ja CGM: hen ja siihen, että näyttää olevan horisontissa lähiaikoina Animas Vibe (joka sai eurooppalaista hyväksyntää jo kesällä 2011.) Dexcom G4: n viime vuoden jännittävä hyväksyntä Platinum CGM, Viben viimeinen kappale näytti pudonneen paikalleen. Yrityksen virkamiehet sanoivat odottaneet G4: n hyväksyntää toimittaakseen päivitetyn Vibe FDA: lle hyväksyttäväksi.
No, niin ei ole vielä tapahtunut. Maailmanlaajuinen viestinnän johtaja Caroline Pavis Animaksssa kertoo meille tämän:
"Animas Vibe
Yhdysvaltojen ja Kanadan tuominen on yksi korkeimmista tavoitteistamme. Olemme sitoutuneet lähettämään PMA: n (markkinoille saattamista edeltävä hyväksyntäpyyntö) Animas Vibe -glukoosin hallintajärjestelmälle mahdollisimman pian vuonna 2013. "
"Call service alarm" toteutuu. Niinpä noin kolme vuotta ennen kuin tämä ongelma ilmenee, että pumppu, joka on äskettäin lopetettu Yhdysvalloissa ja Kanadassa, Animas varoittaa kaikkia, ja huomauttaa, että tuotetunnistetta päivitetään vastaamaan tätä ongelmaa. Mikään ei vaikuta pumpputoimintoihin ennen vuotta 2016, joten pumppujen ei tarvitse tehdä mitään nyt, ja ennen uuden pumpun korvaava takuuaikaa kunnioitetaan.
On liian huonoa, että samaa ennakoivaa viestintää ei sovelleta Animas Vibe -ohjelmaan eikä arkistointiin, joka on "todennäköistä" tapahtumassa tämän vuoden alkupuoliskolla, meille kerrotaan.
Asante Pearl Pump
Pieni on tapahtunut Sunnyvale, CA-pohjaisen Asante Solutionsin kanssa, koska se sai toukokuussa 2011 FDA: n hyväksynnän uudelle osittain kertakäyttöiselle insuliinipumpulle. Asante Pearl oli odotettavissa olevan markkinoilla jo nyt , mutta se ei ole tullut. Näimme Asantea esityksessä kesäkuussa ADA: n tieteellisten istuntojen aikana, ja he ovat palkanneet myös uusia johtajia vuoden 2012 aikana.Mutta ei ole ollut paljon muuta heistä …
Kun kysymys on, yhtiön tiedottaja Steve Bubrick kertoo meille, että Asante odottaa, että Pearl Pump käynnistyy pienessä mittakaavassa vuoden 2013 puoliväliin mennessä. "saat resepti oikein." He ovat rakentaneet varastoja ja valmistautumassa lähestyviin laukaisuihin, hän sanoo.

Vakuutuksen pitäisi kattaa tämä pumppu aivan kuten mikä tahansa muu, Bubrick sanoi. Kustannukset ovat samankaltaiset kuin OmniPod, paitsi että hän kuvailee sitä "edullisemmaksi laitteeksi", koska sinun ei tarvitse vaihtaa kasettia niin usein kuin sinun on vaihdettava pod. Yhtiö aikoo myydä Pearl-pumput DME: n (kestävien lääkinnällisten laitteiden) jakelijoiden kautta voidakseen hyödyntää nykyisiä pumppussopimuksia, joten potilaan vakuutusturva säilyisi ennallaan.
Asante aikoo lähikuukausina aloittaa pumpun markkinoinnin aktiivisesti ja käynnistää sen verkkosivuston uudelleen. Mitä tulee tulevaisuuteen, Bubrick sanoo, että heillä on silmällä CGM-integraatiota, kuten jokainen muu D-laitteen valmistaja. Tällä hetkellä ei ole päätetty eikä ilmoitettu mitään, mutta hän väittää, että Asante pumppaa ja CGM-integraatio "tulee olemaan seuraavan sukupolven painopiste."
Insuletin Next-Gen OmniPodOn vaikea ha
joulukuun puolivälissä uutiset seuraavan sukupolven OmniPodista saadakseen FDA: n hyväksynnän. Pienempi, tyylikäs, ohuempi. Mutta kun tämä este ratkeaa, kuinka kauan kestää uusimmat pods päästä PWDs? Insulet on päivittänyt verkkosivustoaan säännöllisesti, ja nyt aikataulu näyttää helmikuun lopulta tai maaliskuun loppuun mennessä. Mutta jotkut ihmiset ovat kuulleet muita päivämääriä, kuten jotkut lapset Diabetes D-vanhemmilla, jotka sanovat foorumeilla, että heille on kerrottu, että uusin pumppu ei ole käytettävissä vasta huhtikuussa.
Yrityksen PR-edustaja Stephanie Marks sanoo, että aikajanalla ei ole muuttunut mitään, ja että uusia palkoja odotetaan edelleen saatavana maaliskuun loppuun mennessä. Ehkä nämä vanhemmat viittasivat päivitetyn PDM: n (ohjaimen) sijaan pikemminkin uusiin podiineihin? Marks sanoo, ettei hän tiedä eri päivämääriä.

Kesäkuussa 2012 Medtronic toimitti seuraavan gen pump-CGM-järjestelmän FDA: lle arviointia varten.Euroopassa tunnetulla Medtronic Veo -pumpulla (saatavilla vuodesta 2009 lähtien), tällä pumpulla on Low Glucose Suspend (LGS) -ominaisuus, joka käyttää CGM-teknologiaa ihmisen alhaisen verensokerin havaitsemiseen ja keskeyttää automaattisesti insuliinin toimituksen enintään kahdelle tunteja, jos he eivät vastaa hälytyksiin. Tämä on seuraava askel kohti keinotekoista haima-ainetta, ja yhteisöllämme on ollut innoissaan ennakoimassa tätä älykkäämpiä pumppua saapumassa U. S.
Uusi pumppu sisältää kauan odotetun seuraavan sukupolven CGM-anturin nimeltä Enlite (saatavana ulkomailta vuodesta 2011). Ne meistä, jotka ovat käyttäneet nykyistä Medtronic CGM -anturia, viittaavat siihen "harpooniksi", koska se käyttää pitkää neulaa, joka voi usein olla hieman tuskallista pistoksessa ja sitten floppi ja vetää hieman kulumisen aikana. Joten olemme hämmentyneitä tästä uudesta Enlite-anturista
, joka oletettavasti on vähemmän tuskallista, tarkempaa ja kuuden päivän kulutusaika on kolme.
Medtronic toimitti uuden pumpun ja anturin järjestelmäpaketiksi viime kesänä nimellä Medtronic 530G (tarttuva nimi, ay? NOT).

Tämä voi kuitenkin tarkoittaa kaikkea.
Medtronicin viime vuoden lopulla tekemä edistäminen auttoi polttoainetta. Tämä uusi ohjelma takaa, että tämä ohjelma kannusti ihmisiä ostamaan viimeisimmän Paradigm Revel -insuliinin (523 tai 723) insuliinipumpun 15.11.-31.12.2012 välisenä aikana ja takaa vapaan päivityksen uusimpaan pumppujärjestelmään ennen huhtikuun 13, 2013. Ongelma siitä? No niin, nyt Revel IS on viimeisin ja nykyisin käytössä oleva pumppumalli - joten ostaisit uusimman mallin, mikä on periaatteessa väärä päivitystakuu. JOS 530G: n hyväksyntä hyväksytään ennen huhtikuun ajaksi ja Medtronic on antanut sen käyttöön tämän takuun täyttämiseksi.
Hmmm … ehkä Medtronic tietää jotain, jota he eivät ole vielä kertoneet meille. Joten kysyimme.
Valitettavasti, kuten muutkin D-laiteyritykset, Medtronic ei sano paljon virallisesti, mikä tarkoittaa kaikkeaHe eivät voi kommentoida mitään odottavia FDA: n hyväksyntää. Mutta entä uusi tekninen takuu ennen huhtikuun puolivälissä 2013?

PR-johtaja Amanda Sheldon kirjoittaa: "
Käy läpi monenlaisia ylennyksiä koko vuoden ajan … Suoritimme tämän vuoden lopun edistämisen, jotta potilaat voisivat hyödyntää vuoden lopun verovähennyksiä tai muita (koska pumput ovat neljän vuoden takuita). Ajanjaksoa kohti jokaisella promootioilla täytyy olla alkamis- ja päättymispäivä, ja meillä on aloituspäivä. päivämäärä vuoden lopussa edellä mainituista syistä. Ylennykseen osallistuneiden asiakkaiden lukumäärää koskevat tiedot ovat luottamuksellisia."
Roche Diabetes Solo Micropump > Lähes kolme vuotta sitten Roche Diabetes osti Medingo Solo Micropumpin. Sitä ei ole juurikaan sanottu, mutta toistuvien viivästysten vuoksi
tuote on valmis täällä Yhdysvalloissa. Roche Diabetes Social Media -kokouksessa Elokuussa saimme tietää, että huolimatta FDA: n alkuperäisen Solo-pumpun hyväksymisestä, Roche ei aikonut kaupallisesti myydä alkuperäistä laitetta, koska sillä ei ollut integroitua verensokeri-monitoria tai CGM-integraatiota. Vaikuttaa siltä, että he eivät voineet kilpailla nykyisten korjauspumpujen (OmniPod!) Kanssa ilman näitä ominaisuuksia.
Yrityksen tiedottaja Rob Muller kertoo, että Soloista ei ole mitään uutta kertomusta elokuusta 2012 pidetystä huippukokouksesta.
Muut yrityksen johtajat ovat myös olleet tiukkoja, kun jokin Solo-malli saattaa tulla markkinoille U.ssa, mutta he ovat viitanneet siihen, että tulevaisuus voitaisiin nähdä katsomalla Eurooppaa; uusin mallipumppujärjestelmä, joka odotettiin ulkomaille vuonna 2013, todennäköisesti sisältää sisäänrakennetun boluslaskimen ja pystyy lukemaan CGM-tiedot.

Toivottavasti näemme nopean käännöksen viranomaishyväksynnästä ja osa näistä D-laitteista on valmis U.S.PWD: n käyttöön jo kauan! Loppujen lopuksi on meidän (terveys) kellot, jotka ryntävät äänekkäästi.
Vastuuvapauslauseke
: Diabetes Mine -ryhmän luoma sisältö. Lisätietoja saat klikkaamalla tästä.
Vastuuvapauslauseke
Tämä sisältö on luotu Diabetes Mine -verkostoon, joka on diabetesta käsittelevä yhteisö. Sisältöä ei ole tarkistettu lääketieteellisesti eikä se noudata Terveysalan toimituksellisia ohjeita. Lisätietoja Terveysn yhteistyöstä Diabetes Mine -yrityksen kanssa saat napsauttamalla tästä.




